2025年08月30日,上海交通大學章雪晴團隊與新澤西理工學院許曉陽團隊在期刊《Nature Communications》上發表題為" Modulating tumor collagen fiber alignment for enhanced lung cancer immunotherapy via inhaled RNA "的研究論文。

在該研究中,借助艾特森MPE-L2型微流控制備儀,研發團隊開發出一種吸入式RNA納米顆粒,通過局部遞送mRNA和siRNA,同步破壞膠原結構并阻斷免疫抑制,為增強肺癌免疫治療提供了新策略。

研究背景
肺癌免疫治療的臨床效果受限于腫瘤微環境(TME)的雙重阻礙:一是細胞外基質中致密排列的膠原纖維形成物理屏障,排斥腫瘤浸潤T細胞;二是PD-1/PD-L1通路介導的免疫抑制微環境,削弱免疫細胞功能。同時,傳統給藥方式肺靶向性不足,導致藥物在肺部富集度低、全身安全性風險高,進一步制約了治療效能。
1. mscFv/siPD-L1@LNP納米粒作用機制
研究團隊設計了一種可吸入的脂質納米顆粒(LNP),同時攜帶兩種RNA:
?mRNA:編碼抗盤狀結構域受體1(DDR1,一種受體酪氨酸激酶)的單鏈抗體(scFv),用于阻斷膠原纖維排列;
?siRNA:靶向PD-L1,抑制其表達,解除免疫抑制。
通過霧化吸入方式,LNP可直接富集在肺部,被腫瘤細胞攝取后分別表達scFv和沉默PD-L1,實現“雙管齊下”的TME重塑。
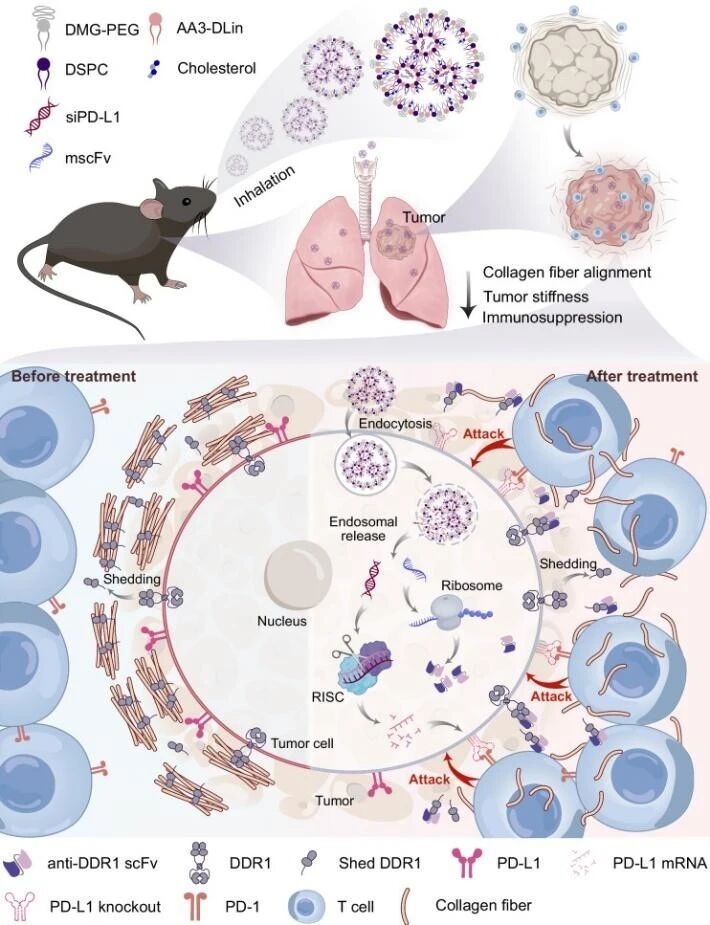
圖例1:mscFv/siPD-L1@LNP納米粒作用機制圖
2. mscFv/siPD-L1@LNP制備工藝條件

圖例2:mscFv/siPD-L1@LNP制備工藝條件
3. mscFv/siPD-L1@LNP的理化性質及藥物遞送效率
首先,mscFv/siPD-L1@LNP在物化前后其物理性質、細胞攝取、基因遞送與沉默效率均保持穩定,且在細胞和體內均能高效遞送藥物,抗DDR1 scFv可在肺部持續表達并對正常細胞無毒性。

圖例3:mscFv/siPD-L1@LNP的理化性質及藥物遞送效率
4. 體外抗腫瘤效果驗證
接著,通過體外共培養實驗,證明mscFv/siPD-L1@LNP能顯著促進腫瘤細胞凋亡,增強CD8+T細胞細胞因子分泌,提升體外抗腫瘤活性。
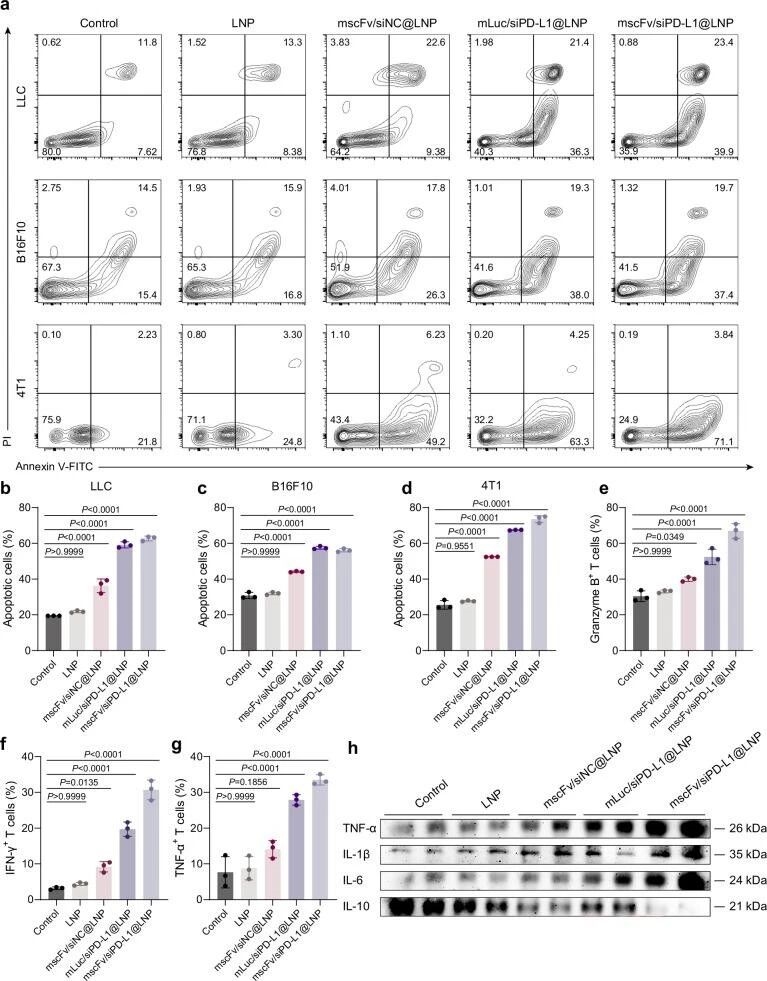
圖例4:體外抗腫瘤效果驗證
5.mscFv對膠原纖維及免疫浸潤的調控
然后,聚焦于mscFv的單獨作用,證明其可重構膠原纖維排列、降低腫瘤硬度,且能劑量依賴性促進免疫細胞浸潤至腫瘤微環境。

圖例5:mscFv對膠原纖維及免疫浸潤的調控
6. 原位肺癌模型中的治療效果
隨后,在原位肺癌小鼠模型中,證明吸入該LNP可顯著抑制腫瘤生長、減輕腫瘤負荷,延長小鼠生存期,且能重塑膠原纖維結構、沉默PD-L1表達。
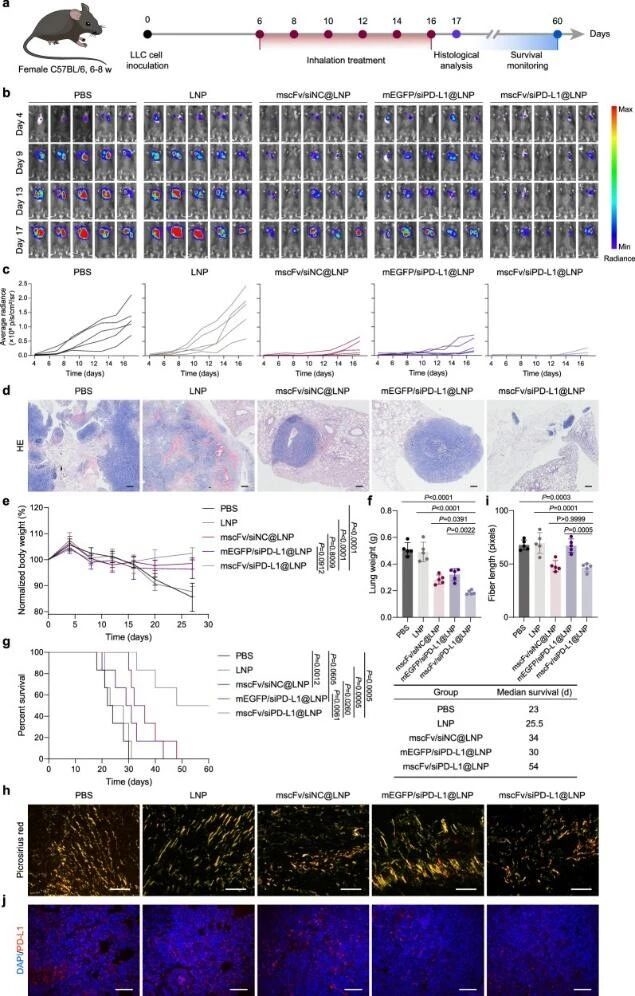
圖例6:原位肺癌模型中的治療效果
7. 原位肺癌模型的TME重塑效果
再者,深入分析原位腫瘤模型的TME變化,證明該療法可增加CD8+T細胞比例及功能,減少免疫抑制細胞,上調促炎因子、下調抑炎因子,實現TME的雙重重塑。

圖例7:原位肺癌模型的TME重塑效果
8. 乳腺癌肺轉移模型中的治療效果
最后,在乳腺癌肺轉移模型中,證明該吸入式療法同樣能抑制腫瘤轉移、減少轉移灶數量,延長生存期,且通過調控TME中免疫細胞浸潤發揮作用。

圖例8:乳腺癌肺轉移模型中的治療效果
知識分享:研究亮點
1 作者成功開發創新的吸入式脂質納米顆粒(LNP)遞送平臺,可同步將編碼抗DDR1單鏈可變片段(scFv)的mRNA與靶向PD-L1的小干擾RNA(siPD-L1)遞送至肺癌細胞。
2 該平臺通過抗DDR1 scFv破壞腫瘤膠原纖維排列、降低腫瘤硬度以瓦解物理屏障,同時借助siPD-L1敲低PD-L1逆轉免疫抑制微環境,雙重作用下有效促進免疫細胞浸潤并恢復其功能,在肺癌原位及轉移小鼠模型中顯著抑制腫瘤生長、延長小鼠生存期。
3 該研究為解決實體瘤免疫治療中免疫排斥與免疫抑制難題提供了高效、低毒的局部聯合治療方案,為提升實體瘤免疫治療效果提供新方向。
參考文獻:
Nature Communications (IF 15.7) Pub Date:2025-08-30,DOI:10.1038/s41467-025-63415-0.
 歡迎來到蘇州艾特森制藥設備有限公司網站!
歡迎來到蘇州艾特森制藥設備有限公司網站! 歡迎來到蘇州艾特森制藥設備有限公司網站!
歡迎來到蘇州艾特森制藥設備有限公司網站!









